【FDA PPT 译文 】通过模型整合实证的方法助力仿制药的开发
2021-07-08 11:06:51
导 读
FDA仿制药办公室的定量方法与建模部主任Liang Zhao博士,于2021年6月的2021年仿制药科学与研究计划研讨会上,做了《通过模型整合实证的方法助力仿制药的开发》Model-Integrated Evidence for Generic Drug Development的报告。
Liang Zhao博士概述了目前模型整合实证方法的新技术和应用场景,同时讲解了该研讨会期间其他科学家在该领域涉及到的一些演讲。
凡默谷技术团队翻译了该PPT,希望对您的建模业务有帮助。
报告人
Liang Zhao(赵亮)博士,FDA仿制药办公室定量方法与建模部
赵博士于2009年加入FDA,先在临床药理部门工作6年,从2015年开始担任仿制药办公室定量方法与建模部主任。在加入FDA之前,赵博士曾就职于BMS和Medlmmune等制药企业。他在中国药科大学获得学士学位,在上海医科大学获得硕士学位,在美国The Ohio State University获得博士学位。
内 容
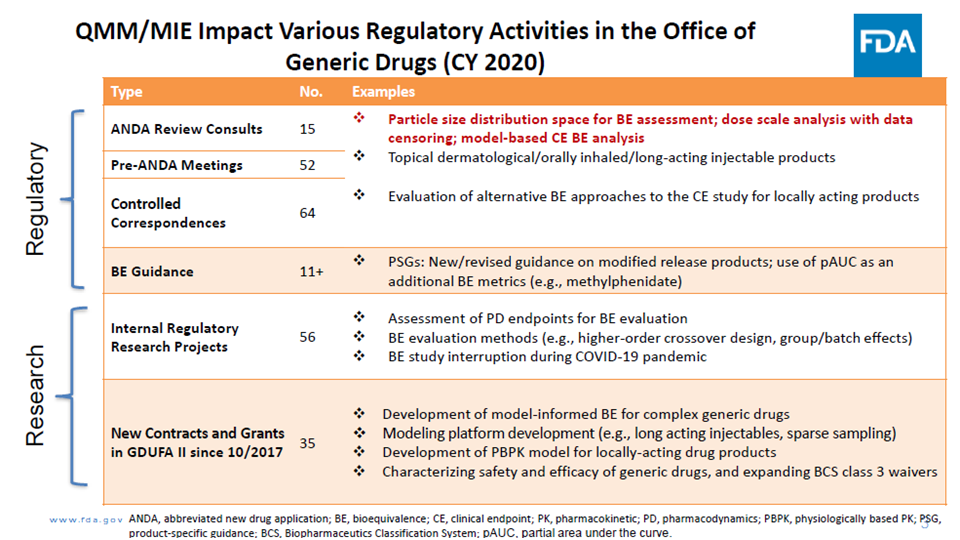
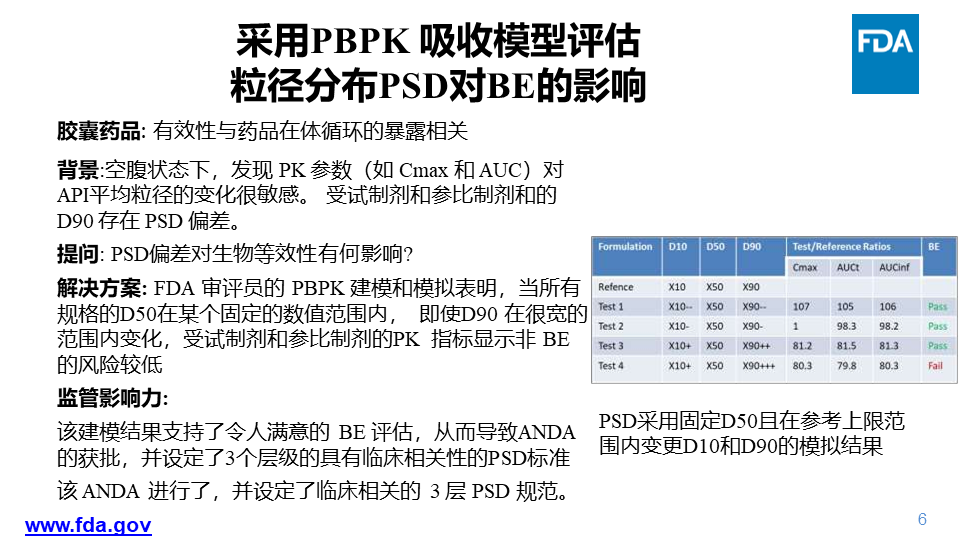
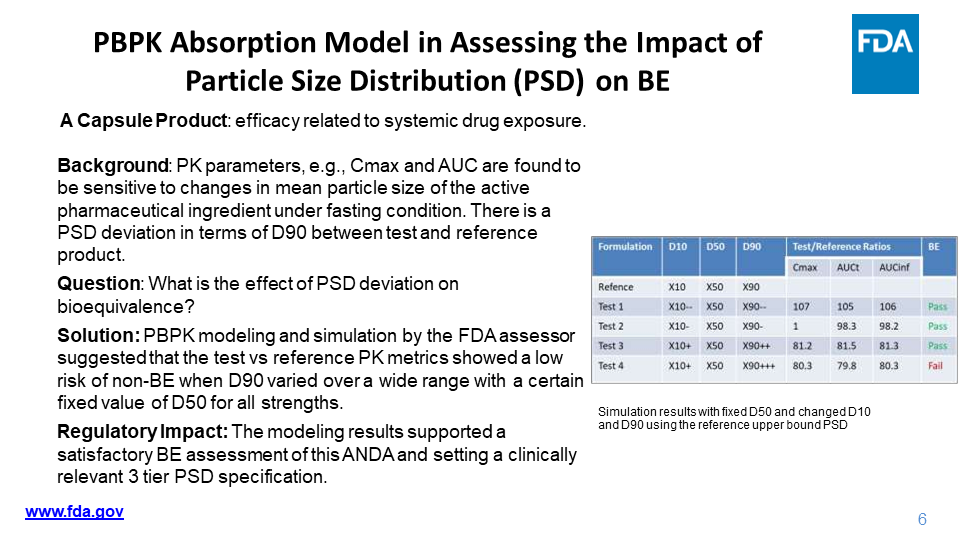
赵博士首先介绍了模型整合实证MIE的理念和应用场景。接着从监管审评和监管科学研究两个维度讲解了2020年QMM/MIE 影响FDA仿制药办公室的法规监管活动,例如用于评估BE的粒径分布的安全空间,推进复杂药品的 QMM/MIE方法,指导BE指导原则的撰写,新的BE评估方法,COVID-19大流行期间 BE 研究中断后如何处理等。最后讲解了该领域相关的GDUFA监管科学研究项目进展,例如,新的替代性BE指标,BCS 3类药物的生物豁免,食物对BE的影响,通过模型制定药品BE的安全空间,新的BE试验设计。
对应的PPT中文译文和原稿如下: